La prophylaxie préexposition (PPrE) est une modalité hautement efficace pour la prévention du VIH qui peut être prescrite par les omnipraticiens.
La prophylaxie préexposition devrait être offerte aux patients à risque élevé d’exposition au VIH, y compris les hommes gais, bisexuels et autres hommes ayant des relations sexuelles avec des hommes (HGB), les femmes ayant des rapports non protégés avec des partenaires dont le statut à l’égard d’un VIH transmissible est confirmé ou inconnu et les personnes qui utilisent des drogues par injection et partagent du matériel pour injection.
La PPrE en prise orale quotidienne (fumarate de ténofovir disoproxil/emtricitabine [TDF/FTC] ou fumarate de ténofovir alafénamide/emtricitabine en comprimés) est approuvée par Santé Canada.
Le schéma TDF/FTC à la demande peut être prescrit aux hommes gais, bisexuels et autres hommes ayant des relations sexuelles avec des hommes (HGB) et a une efficacité similaire.
La ligne directrice canadienne décrit avec précision le protocole de surveillance de la PPrE, y compris : dépistage du VIH, dépistage des ITS et surveillance rénale.
L’incidence du virus de l’immunodéficience humaine (VIH) est en hausse au Canada. L’Agence de la santé publique du Canada a estimé à 2242 le nombre de nouveaux cas de VIH déclarés en 2018, ce qui rappelle la nécessité d’adopter des stratégies détaillées et complètes de prévention1. La prophylaxie préexposition (PPrE) est une importante façon de prévenir l’acquisition du VIH, mais elle est sous-utilisée2–4. Même si les généralistes (p. ex., médecins de famille, infirmières praticiennes et internistes généraux) peuvent jouer un rôle vital dans l’adoption de la PPrE, une récente enquête de petite taille menée auprès d’omnipraticiens néo-écossais a révélé que la plupart ne prescrivaient pas la PPrE5. Nous décrivons la PPrE au VIH, nous faisons le point sur son utilisation actuelle et sur les obstacles potentiels à son utilisation, et proposons une approche à sa prescription (encadré 1).
Encadré 1: Données utilisées pour la présente revueNous avons réalisé une interrogation du réseau PubMed sur les recherches originales et les articles de revues publiés entre janvier 2017 et janvier 2021, à partir des termes « HIV PrEP » ou « HIV pre-exposure prophylaxis » et « Canada » ou « Canadian ». Nous avons utilisé cet intervalle de temps parce que la ligne directrice canadienne sur la prophylaxie préexposition (PPrE) a été émise en 2017. Nous avons également passé en revue les lignes directrices sur la PPrE actuellement en vigueur au Canada et aux États-Unis. Nous avons sélectionné les études pertinentes et procédé à une interrogation manuelle de leurs listes bibliographiques pour trouver d’autres articles.
Qu’est-ce que la prophylaxie préexposition au VIH?La prophylaxie préexposition au VIH repose sur l’utilisation d’antirétroviraux chez des personnes de statut VIH négatif; elle commence avant et continue après de potentielles expositions au VIH afin d’en prévenir l’acquisition6,7. Elle peut être prise en continu (sur une base quotidienne) ou à la demande avant une exposition probable6,7. La prophylaxie préexposition est utilisée à meilleur escient dans le cadre d’une stratégie détaillée et complète concernant la santé sexuelle et le VIH, incluant l’éducation à la réduction des préjudices, le dépistage des infections transmissibles sexuellement (ITS), des mesures en santé génésique et mentale et la surveillance des comorbidités, comme l’hépatite B ou la dépression.
Quelle est l’efficacité de la prophylaxie préexposition au VIH?Des données probantes de grande qualité tirées d’essais randomisés et contrôlés (ERC) et d’études d’observation ont montré que l’utilisation quotidienne de la PPrE chez les hommes gais, bisexuels et autres hommes ayant des relations sexuelles avec des hommes (HGB) prévient à près de 100 % l’acquisition de VIH lorsque l’observance thérapeutique est élevée8–10. Des données probantes de grande qualité en ont montré l’efficacité à 95 % lors d’expositions hétérosexuelles, selon le degré d’observance thérapeutique11–13. Un ERC de 2013 sur des utilisateurs de drogues par injection à Bangkok, en Thaïlande (Bangkok Tenofovir Study) a fait état d’une efficacité de 48,9 % avec la PPrE, mais l’observance thérapeutique des participants y était très faible; l’efficacité passait à 74 % dans un sous-groupe de participants qui présentaient des taux détectables d’antiviraux14. La recherche, toutes populations confondues, a montré l’importance pour l’efficacité de l’observance thérapeutique, et des données observationnelles en ont confirmé la grande efficacité en contexte réel, les infections perthérapeutiques ayant été très rares15. L’adoption de la PPrE a été clairement associée à un déclin des diagnostics de VIH à l’échelle des populations16,17.
L’essai IPERGAY (Intervention préventive de l’exposition aux risques avec et pour les gais) a montré que la PPrE à la demande est efficace chez les HGB, avec une réduction de 86 % du risque d’acquisition du VIH; seulement 2 infections perthérapeutiques sont survenues chez 2 participants dont l’observance thérapeutique à l’égard du schéma prophylactique laissait à désirer6,18. Les participants ont pris un nombre médian de 15 comprimés par mois et, même si une analyse post hoc a montré une efficacité similaire chez les participants qui utilisaient moins de 15 comprimés par mois, on dispose encore de données limitées quant à l’efficacité lors d’expositions plus sporadiques18,19.
Qui est candidat à la prophylaxie préexposition au VIH?Le risque d’acquisition du VIH dépend de la probabilité que le partenaire ait une infection au VIH transmissible et du type d’exposition (encadré 2). Plusieurs études ont montré qu’une personne de statut VIH positif sous antirétroviraux ayant une charge virale inférieure à 200 copies/mL ne peut pas transmettre le VIH à ses partenaires sexuels20–22. L’indication de la PPrE se fonde sur la probabilité d’un risque élevé d’exposition à un VIH transmissible6.
Encadré 2: Risque de transmission selon le type d’exposition6Risque qu’une personne ait une infection au VIH transmissible
Substantiel
Statut VIH positif et charge virale > 40 copies/mL
Statut VIH inconnu, mais appartenant à une population où la prévalence du VIH est élevée
Faible, mais non nul
Négligeable ou nul
Statut VIH négatif confirmé
Statut VIH positif, charge virale < 40 copies/mL confirmée et absence d’infection transmissible sexuellement au moment de l’exposition
Statut VIH inconnu, population générale
Risque de transmission selon le type d’exposition à une source dont le statut est VIH positif
Élevé
Relation anale passive
Partage d’aiguilles
Modéré
Faible
Relation sexuelle orale active
Relation sexuelle orale passive
Contact oral–anal
Partage de jouets sexuels
Contact sanguin sur peau lésée
Des lignes directrices ont été publiées (p. ex., celles des Centers for Disease Control and Prevention [CDC]; figure 1) pour faciliter l’identification des meilleurs candidats à la PPrE. Les recommandations doivent cependant tenir compte des facteurs de risque individuels et de l’épidémiologie locale, et se veulent des outils plutôt que des règles rigides. Un processus de décision partagée avec le patient est essentiel et on ne doit pas refuser la PPrE aux patients, même s’ils se considèrent eux-mêmes comme à risque à l’égard du VIH en n’appliquant pas les mesures générales de prévention6,7.
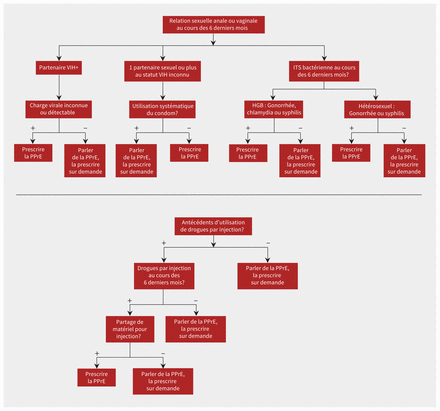
 Figure 1:
Figure 1: Algorithme de la prophylaxie préexposition (PPrE) selon la ligne directrice des CDC6. Remarque : CDC = Centers for Disease Control and Prevention, HGB = hommes gais, bisexuels ou ayant des relations avec des hommes, ITS = infection transmissible sexuellement.
Les lignes directrices canadiennes et américaines au sujet de la PPrE diffèrent légèrement, mais de manière générale, la PPrE est recommandée aux personnes qui ont des relations sexuelles anales ou vaginales sans condom avec des partenaires dont elles ignorent le statut VIH ou des partenaires porteurs connus d’un VIH transmissible (c.-à-d., charge virale inconnue ou détectable)6,7,23. D’autres facteurs de risque, comme le fait d’avoir déjà utilisé la prophylaxie postexposition au VIH ou contracté certaines ITS bactériennes (figure 1), sont aussi utiles pour reconnaître les personnes exposées à un risque élevé d’exposition au VIH6,7,23. Des outils de stratification du risque (p. ex., l’indice HIRIMSM [indice du risque d’incidence du VIH chez les HGB]) peuvent aussi aider les professionnels de la santé à reconnaître les patients exposés à un risque élevé à l’égard du VIH6.
La PPrE à la demande peut être considérée comme une solution de rechange efficace chez les HGB ou les femmes transgenres qui ne souhaitent pas prendre de comprimés tous les jours ou dont le nombre d’expositions potentielles chaque mois est peu élevé6. Elle n’est pas recommandée d’emblée chez d’autres populations en raison d’un manque de données probantes.
Les lignes directrices canadiennes et américaines ont recommandé la PPrE chez les patients qui partagent du matériel pour les injections6,7. Des outils de stratification du risque pour les personnes qui utilisent des drogues par injection ont été créés; par exemple, l’outil de dépistage ARCHIDU (Assessing the Risk of Contracting HIV in Injection Drug Users)24.
Comment prescrit-on et surveille-t-on la prophylaxie préexposition?Les schémas quotidiens de PPrE actuellement offerts (tableau 1) sont les comprimés d’association de fumarate de ténofovir disoproxil/ emtricitabine (TDF/FTC) ou de fumarate de ténofovir alafénamide/ emtricitabine (TAF/FTC) à prise quotidienne6,7,23,25. La PPrE à la demande, aussi connue sous le nom PPrE « 2-1-1 », se compose de 2 comprimés pris de 2–24 heures avant une relation sexuelle non protégée suivis de 1 comprimé par jour pendant 48 heures après le dernier contact sexuel6,7. Des préparations de PPrE à action prolongée ont aussi été conçues, comme le cabotégravir en suspension injectable, administré toutes les 8 semaines. Même s’il n’est pas encore approuvé pour la PPrE au Canada, il pourrait éventuellement être envisagé chez les personnes qui préfèrent ces injections à une prise quotidienne de comprimés26.
Tableau 1:Schéma de prophylaxie préexposition au VIH6,7
Les prescripteurs doivent procéder à des évaluations avant le début de la PPrE, puis tous les 3 mois pendant la durée du traitement prophylactique (tableau 2)6,7. Ces évaluations sont l’occasion de vérifier si la PPrE est toujours indiquée et de rappeler l’importance de l’observance thérapeutique. Un dépistage trimestriel du VIH est important parce que l’utilisation prolongée de la PPrE chez les patients au statut VIH négatif peut éventuellement entraîner une résistance aux médicaments27.
Tableau 2:Surveillance recommandée des patients sous prophylaxie préexposition au VIH6,7
La prophylaxie préexposition doit faire partie intégrante d’une approche détaillée et complète en santé sexuelle et VIH, et inclure l’éducation, le dépistage des ITS et la prise en charge de la santé génésique, aussi bien que la réduction des préjudices et l’évaluation et la prise en charge des problèmes de santé mentale.
On associe parfois les 2 préparations de PPrE à de légers effets gastro-intestinaux indésirables, mais ces symptômes rentrent rapidement dans l’ordre et justifient rarement l’arrêt de la PPrE28. Le fumarate de ténofovir disoproxil est associé à un faible risque de toxicité rénale et à une légère baisse de la densité minérale osseuse, qui sont tous deux habituellement réversibles à l’arrêt de la prise du médicament28,29. Le fumarate de ténofovir alafénamide a pour sa part été associé à une augmentation plus marquée des triglycérides et du gain pondéral par rapport au TDF30. Chez la plupart des gens à risque à l’égard du VIH, les bienfaits d’une prévention efficace du VIH surclassent les inconvénients associés aux effets indésirables du traitement.
On peut prescrire le fumarate de ténofovir disoproxil/emtricitabine en PPrE chez les personnes enceintes ou qui allaitent6,7,23. Ce médicament a été largement utilisé pour le traitement du VIH durant la grossesse sans issues négatives et les lignes directrices du CDC mises à jour en 2021, de même qu’une analyse de 2019 sur l’administration de la PPrE chez des femmes enceintes et en période postpartum au Kenya occidental n’ont mentionné aucune différence quant à l’issue des grossesses chez les femmes sous PPrE périnatale7,31.
Les schémas de fumarate de ténofovir disoproxil/emtricitabine et de TAF/FTC agissent également contre le virus de l’hépatite B (VHB) et si la prise de ces médicaments est cessée, les patients porteurs d’une infection au VHB peuvent avoir des poussées d’hépatite6,7. Cela rappelle l’importance du dépistage du VHB au départ et de la vaccination chez les patients qui ne sont pas protégés contre ce virus. Lorsqu’on débute la PPrE au VIH chez les patients porteurs d’une infection chronique au VHB, il agit également comme traitement du VHB et conformément aux lignes directrices, requiert une surveillance, en consultation avec un professionnel spécialiste du VHB, au besoin6,7.
Les adolescents qui pèsent moins de 35 kg peuvent aussi prendre sans danger la PPrE par TDF/FTC ou TAF/FTC7.
Quelle proportion de la population canadienne admissible utilise la prophylaxie préexposition?Étant donné qu’au Canada, il n’existe pas de système national de surveillance de la PPrE, elle est difficile à quantifier. Toutefois, l’utilisation est probablement en hausse. La prophylaxie préexposition a été utilisée hors indication jusqu’à l’approbation par Santé Canada du schéma TDF/FTC quotidien pour la PPrE en 2016, des versions génériques à moindre coût ont fait leur entrée sur le marché en 2017 et les lignes directrices canadiennes ont été publiées en 20172,6,32.
Selon les estimations d’une étude sur les données relatives aux ordonnances rédigées dans 8 provinces, 9657 patients ont pris la PPrE en 2018, dont environ 98 % se déclaraient de sexe masculin32. Entre 2017 et 2019, l’admissibilité à la PPrE en vertu des lignes directrices canadiennes pour les HGB dans les grands centres urbains variait de 44,9 %–58,1 %, et pourtant seulement 14,5 %–21,8 % l’avaient utilisée3. Même parmi les HGB exposés à un risque élevé de VIH, seulement 24,6 % ont pris la PPrE en 20174.
En 2018, les femmes composaient 25 % des nouveaux diagnostics de VIH et ne représentaient pourtant que 2 % de l’ensemble des utilisateurs de PPrE au Canada1,32. On dispose de données minimales sur son adoption dans d’autres populations.
Quels obstacles freinent l’accès à la prophylaxie préexposition?La principale condition préalable à l’adoption de la PPrE est la reconnaissance des patients à risque à l’égard du VIH. Or, le risque de VIH est souvent sous-estimé tant par les patients que par les professionnels de la santé. Étant donné que la majeure partie des efforts déployés pour favoriser l’adoption de la PPrE au Canada et ailleurs ont visé les HGB, le risque est particulièrement sous-évalué dans d’autres groupes; par exemple, chez les femmes, les utilisateurs de drogues par injection et les personnes pour lesquelles les outils validés d’évaluation des risques sont peu nombreux, voire inexistants33,34.
Même chez les patients qui se savent exposés à un risque élevé à l’égard du VIH, on connaît peu et on accepte plus ou moins bien la PPrE, ce qui pose un défi supplémentaire; et la discrimination systémique exacerbe souvent le problème. Par exemple, parmi les HGB, le fait de ne pas être tout à fait « sorti du placard » ou de ne pas s’identifier en tant que gai a été lié à une sensibilisation, une connaissance et une adoption moins grandes de la PPrE en raison de l’inconfort inhérent à la divulgation, de la crainte que la PPrE ne les étiquette en tant qu’HGB; et cela réduit leur accès aux campagnes de sensibilisation à la PPrE3,4,35. S’identifier en tant que personne noire, autochtone ou d’un autre groupe racialisé a aussi été associé à une sensibilisation et à une connaissance moindres de la PPrE4,36. Une analyse de 2022 fondée sur des entrevues auprès d’HGB noirs à Toronto a révélé que les programmes communautaires ne focalisaient pas sur la PPrE et, même là où elle était publicisée, la PPrE était souvent mal expliquée ou semblait encourager les relations sexuelles non protégées37. Plusieurs communautés se sont dites inquiètes de la stigmatisation rampante qui associe la PPrE à la « promiscuité »37.
Les candidats potentiels à la PPrE doivent trouver un professionnel de la santé qui a les bonnes connaissances, qui se sent à l’aise de discuter de santé sexuelle et qui accepte de prescrire la PPrE. Les difficultés d’accès à un professionnel de soins primaires et le manque d’expérience de nombreux omnipraticiens dans la prescription de la PPrE contribuent au problème; ces défis sont plus aigus en région rurale ou éloignée2–5. Les préjugés des professionnels à l’égard d’un manque prévisible d’observance thérapeutique peuvent aussi causer un accès inéquitable. Il faut dire que la fréquence des visites et des analyses de laboratoire pour la surveillance est fastidieuse, tant pour les patients que pour les professionnels.
L’abordabilité est un autre obstacle important à la PPrE, peu importe la population visée2,37. Même si toutes les provinces et tous les territoires fournissent une certaine couverture de la PPrE, les critères d’admissibilité et l’ampleur de la couverture varient (https://hivclinic.ca/wp-content/uploads/2022/02/2022-Jan_ARV-access-for-PrEP.pdf). La perception même de l’inabordabilité des traitements peut empêcher les patients de demander la PPrE et de s’informer de leur couverture d’assurance37.
Quelles stratégies peut-on employer pour favoriser l’utilisation de la prophylaxie préexposition?Les médecins doivent commencer par parler du risque d’acquisition du VIH et de la PPrE dans le cadre des soins de santé préventifs de routine, afin que les patients n’aient pas à compter sur eux-mêmes pour établir leur risque. En particulier, la discussion sur la PPrE devrait faire partie des soins standard pour les personnes qui présentent des ITS bactériennes ou qui subissent des dépistages d’ITS6,7,38,39. Cela demande la création d’un espace sécuritaire pour aborder le risque de VIH, en luttant proactivement contre l’homophobie et la stigmatisation liées aux comportements sexuels à risque et à l’utilisation de substances psychoactives4. Les professionnels peuvent aussi rendre la PPrE plus acceptable pour les patients en corrigeant l’impression fausse selon laquelle la PPrE est une intervention uniquement destinée aux personnes gaies ou à la sexualité débridée4,34,37.
En tant qu’intervention de prévention primaire relativement simple, la PPrE peut être administrée dans le cadre des soins primaires de routine. Toutefois, pour prescrire la PPrE, les professionnels doivent avoir les connaissances voulues, se sentir à l’aise de parler de santé sexuelle et avoir une compétence culturelle pour travailler auprès de populations historiquement marginalisées40. Les lignes directrices, comme celles des CDC, peuvent aider les médecins à prescrire la PPrE, et des modules de formation médicale continue faciles d’accès ont été créés pour informer les professionnels en santé communautaire (p. ex., https://hivprevention.talentlms.com/shared/start/key:LZGIDNHR)5–7,35.
Des solutions systémiques sont également requises pour les candidats que le contexte des soins primaires ne permet pas d’identifier. Par exemple, des systèmes automatisés peuvent identifier et accélérer les consultations en clinique pour PPrE chez les patients qui présentent des facteurs de risque et qui pourraient par ailleurs passer sous le radar; par exemple, en intégrant des modèles prédictifs dans les dossiers médicaux électroniques lors d’hospitalisations ou en lançant des demandes de consultation automatisées quand des ITS sont signalées à la santé publique4,41,42.
La nature même de la PPrE, dont les protocoles sont très bien établis, permettrait également d’augmenter le nombre de professionnels prescripteurs potentiels en délégant certaines tâches à d’autres professionnels travaillant sous leur supervision. Parmi les exemples de réussite, mentionnons les cliniques communautaires ou de santé sexuelle dirigées par du personnel infirmier, la distribution des médicaments par les pharmaciens et les cliniques mobiles qui offrent une PPrE facile d’accès4,41,43.
La technologie peut aussi servir à améliorer l’accès à la PPrE dans les contextes où les ressources laissent à désirer, ou faciliter la prise de rendez-vous virtuels par télémédecine afin de garantir un contact avec des professionnels dans les régions moins bien desservies43. Les programmes communautaires peuvent de leur côté promouvoir un engagement basé sur la confidance et des interventions culturellement adaptées pour les communautés maginalisées37,43. Les responsables de la santé publique ont aussi la tâche de faire de la sensibilisation sur la PPrE en tant que stratégie préventive sécuritaire et efficace pour de nombreuses populations.
Parmi les plus importantes interventions susceptibles de favoriser l’adoption de la PPrE, mentionnons l’abolition des obstacles de nature économique. Les médecins doivent être au courant des options concernant la couverture des médicaments offerts dans leur région et militer pour une plus grande couverture par les régimes publics là où l’accès n’est pas universel. La PPrE à la demande pourrait aussi réduire les obstacles de nature économique.
ConclusionLa prophylaxie préexposition est une importante modalité de prévention de l’acquisition du VIH qui peut avoir une efficacité de près de 100 % chez les personnes qui ont une bonne observance thérapeutique. Elle doit être utilisée dans le cadre d’une stratégie détaillée et complète de prévention du VIH et les omnipraticiens peuvent jouer un rôle important dans la sensibilisation à cette mesure et son adoption. Les lignes directrices proposent des protocoles faciles à suivre pour reconnaître les patients admissibles, prescrire les médicaments et assurer une surveillance continue. Les obstacles à la PPrE incluent la sous-estimation du risque de VIH dans certaines populations, un manque de sensibilisation à la PPrE, un accès inadéquat aux prescripteurs et le coût des médicaments (encadré 3). La stigmatisation omniprésente et les iniquités structurelles qui freinent l’éducation et les soins exacerbent ces lacunes. Les professionnels de la santé peuvent contribuer à les combler en se renseignant davantage au sujet de la PPrE, en l’abordant de routine avec leurs patients et en se prononçant en faveur de changements systémiques, notamment en ce qui concerne la couverture d’assurance médicaments.
Encadré 3: Questions sans réponsesDe quels outils basés sur des données probantes dispose-t-on pour reconnaître les femmes et les personnes utilisant des drogues par injection qui bénéficieraient le plus de la prophylaxie préexposition (PPrE) dans un pays à revenu élevé comme le Canada?
Comment mieux faire connaître la PPrE et favoriser son adoption dans les communautés déjà confrontées à des obstacles en termes d’accès aux soins de santé?
Quelles sont les stratégies optimales pour mieux faire connaître la PPrE aux professionnels de la santé et les rendre plus à l’aise de la suggérer?
RemerciementsLes auteurs reconnaissent vivre et travailler en territoire traditionnel de plusieurs peuples autochtones, y compris les Abénakis, Anishinabées, Attawandarons, Chippewas, Haudenosaunees, Hurons/Wendats, Kanien’keha:ka, Lūnaapéewaks et Mississaugas de Credit.
FootnotesIntérêts concurrents: Jean-Guy Baril a reçu des honoraires de consultation des sociétés ViiV Healthcare, Merck et Gilead, et des honoraires de conférencier des sociétés Merck et Gilead. Il est également membre de comités consultatifs sur le VIH et le VHC pour le Ministere de la santé du Québec. Mia Biondi a reçu des honoraires de conférenciere de la société Gilead Canada et est contractuelle indépendante pour la société Omega Specialty Nurses. Darrell Tan détient une Chaire de recherche du Canada de niveau 2 en prévention du VIH et en recherche sur les infections transmises sexuellement (ITS). Aucun autre intéret concurrent n’a été déclaré.
Cet article a été commandé et a été révisé par des pairs.
Collaborateurs: Darrell Tan a conçu cette revue. Amanda Hempel a procédé a la revue de la documentation et a rédigé le manuscrit. Tous les auteurs ont relu le manuscrit et en ont révisé de façon critique le contenu intellectuel important; ils ont donné leur approbation finale pour la version destinée a etre publiée et assument l’entiere responsabilité de tous les aspects du travail.
Financement: Jean-Guy Baril a reçu des bourses des sociétés GSK, Merck et Gilead (versées a son établissement). Darrell Tan a reçu des subventions de la société AbbVie (soutien en nature remis a son établissement pour une recherche a initiative de l’investigateur), de la société Gilead (soutien versé a son établissement pour la recherche a l’initiative de l’investigateur) et de la société GSK (soutien a son établissement pour la réalisation d’essais cliniques commandités par l’industrie).
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/
留言 (0)